Батареи – это устройства, которые накапливают и высвобождают энергию путем перемещения заряженных частиц, называемых ионами, между двумя материалами, называемыми электродами. Электроды разделены жидкостью или гелем, называемым электролитом, который содержит ионы и другие молекулы. Когда используется аккумулятор, на поверхности каждого электрода образуется тонкий слой молекул, называемый твердоэлектролитной фазой (SEI).
Литий-ионные аккумуляторы (LIBs) и натрий-ионные аккумуляторы (SIBs) страдают недостаточной обратимостью окислительно-восстановительных процессов на границе раздела электрод/электролит, что связано с образованием механически нестабильных и реактивных SEI. Стабильный, богатый неорганическими веществами SEIs может изолировать перенос электронов, позволяя диффундировать только определенным ионам, тем самым поддерживая обратимый цикл за пределами электрохимического предела электролита.
В то время как электрохимические элементы, использующие неорганические расплавленные солевые электролиты при повышенных температурах (> 100 °C), демонстрируют стабильные циклические характеристики, повседневное применение зависит от электролитов аккумуляторных батарей, содержащих как соли металлов, так и органические растворители. Эта смесь запускает конкурентные реакции на границе раздела заряженных элементов, вызывая постоянный расход электролита и неравномерное осаждение металла, т.е. образование дендритов в
случае металлических электродов, что приводит к выходу батареи из строя, а иногда и к проблемам безопасности.
Одним из наиболее практически масштабируемых способов оптимизации химического состава и морфологии SEI для обратимого переноса заряда является совместный выбор химического состава электролита и протокола формирования (т.е. начальных условий циклирования с конкретными условиями тока/напряжения). В то же время значение материала электрода в этом процессе было заметно недооценено, несмотря на присущее ему влияние на предварительные фазы формирования SEI.
Чтобы восполнить этот информационный пробел, исследователи из Университетов Дикина и Монаша (Мельбурн, Австралия) изучили влияние физико-химических свойств электрода на механизм образования SEI с использованием ионных жидкостей и натриевых электролитов на основе карбоната. Работа опубликована в журнале Energy & Environmental Science.
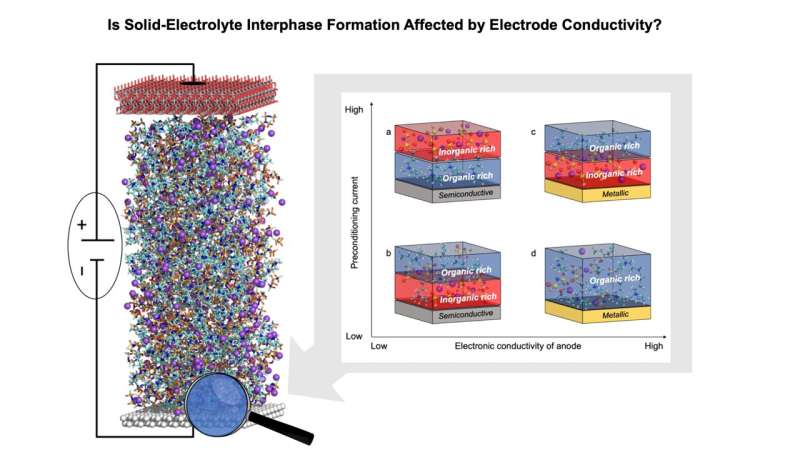
Используя комбинацию экспериментальных и теоретических инструментов, мы продемонстрировали, что структура границы раздела электролит–электрод и свойства раздела твердый электролит существенно зависят от поляризуемости электрода (его диэлектрической природы), и мы объяснили эти явления в контексте способности заряженных электродов адсорбировать разновидности электролита (см. рисунок выше).
В частности, неметаллические электроды со слабыми ван-дер-ваальсовыми силами сталкиваются с электростатическим отталкиванием, предотвращающим накопление высокополярных растворителей или ионов, несущих тот же заряд, что и заряд электрода. Это влияет на концентрацию комплексов Na–аниона с органическим растворителем вблизи заряженного электрода. Следовательно, образующиеся межфазные химические составы варьируются в зависимости от применяемых условий загрузки, что приводит к развитию различных межфазных химических составов — либо полученных на основе растворителя, либо на основе аниона.
Благодаря этому новому научному открытию и знаниям о структуре ионной сольватации в данных электролитах мы можем быть более рациональными при разработке интеллектуальных протоколов циклирования для перезаряжаемых батарей.
Это исследование могло бы помочь в разработке более совершенных аккумуляторов для различных применений, таких как электромобили, хранилища возобновляемой энергии или портативные устройства. Это также могло бы помочь разработать новые способы использования электрохимических систем для других целей, таких как производство химических веществ (электрокатализ) или извлечение металлов из отходов.